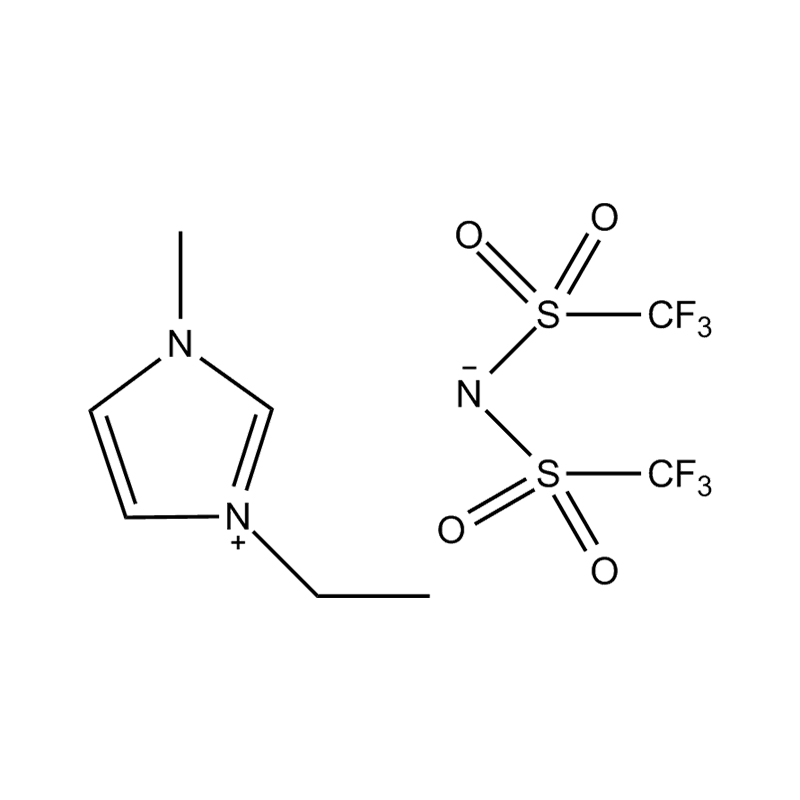
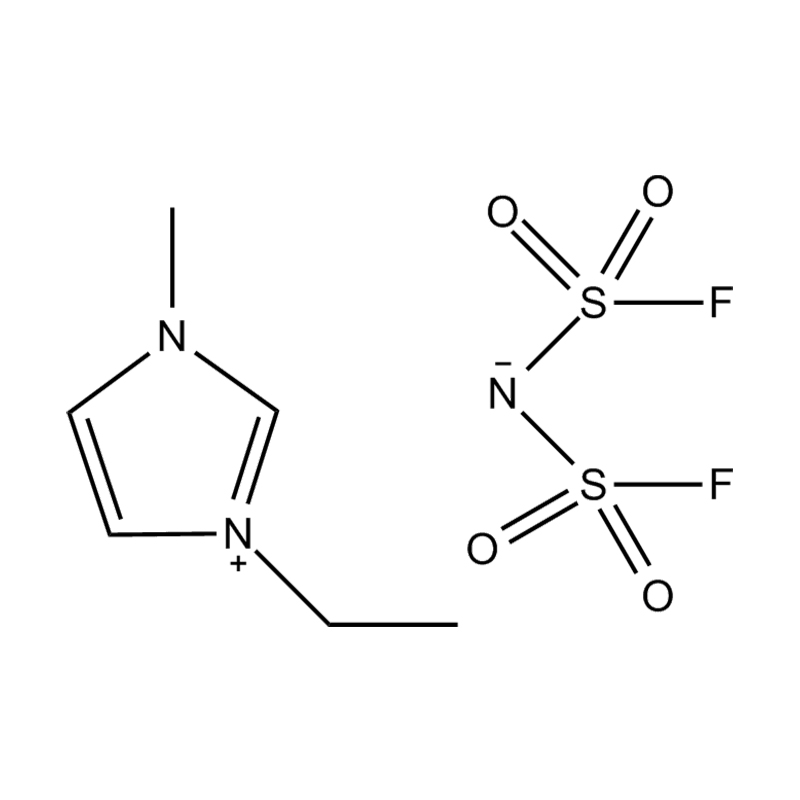
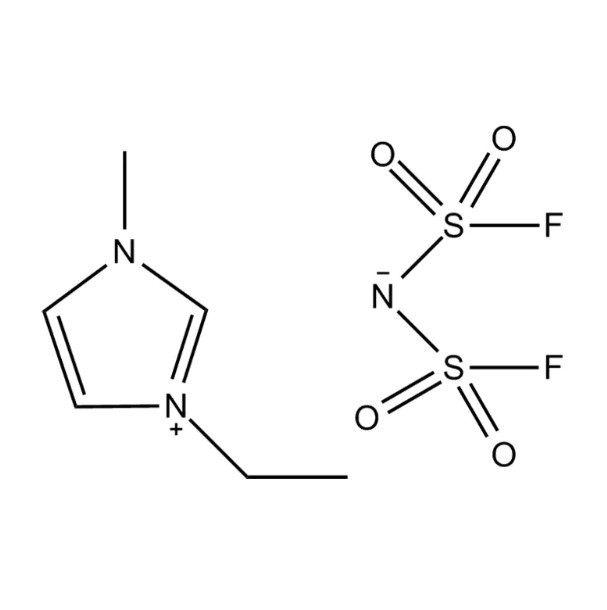
1-Ethyl-3-methylimidazolium-bis(fluorsulfonyl)imid – allgemein als [EMIM][FSI] abgekürzt – ist eine ionische Flüssigkeit, die in den letzten zwei Jahrzehnten intensive wissenschaftliche und industrielle Aufmerksamkeit erregt hat. Ionische Flüssigkeiten sind Salze, die bei oder nahe Raumtemperatur in flüssiger Form vorliegen, und [EMIM][FSI] zeichnet sich innerhalb dieser breiten Familie durch eine außergewöhnliche Kombination von Eigenschaften aus: sehr niedrige Viskosität, breites elektrochemisches Stabilitätsfenster, hohe Ionenleitfähigkeit, vernachlässigbarer Dampfdruck und gute thermische Stabilität. Diese Eigenschaften machen es zu einer der vielseitigsten und praktischsten verfügbaren ionischen Flüssigkeiten mit aktiven Anwendungen in den Bereichen Energiespeicherung, elektrochemische Synthese, Schmierstoffwissenschaft und fortschrittliche Materialforschung.
Content
- 1 Grundlegende physikalische und chemische Eigenschaften, die seine Verwendung ermöglichen
- 2 Elektrolyt in Lithium-Ionen- und Batterien der nächsten Generation
- 3 Superkondensatoren und elektrochemische Kondensatorelektrolyte
- 4 Galvanische Abscheidung von Metallen und Halbleitern
- 5 Verwendung als Lösungsmittel und Reaktionsmedium in der chemischen Synthese
- 6 Schmierung und tribologische Anwendungen
- 7 Zusammenfassung der wichtigsten Anwendungsbereiche
- 8 Handhabung, Sicherheit und praktische Überlegungen
Grundlegende physikalische und chemische Eigenschaften, die seine Verwendung ermöglichen
Um zu verstehen, warum [EMIM][FSI] so weit verbreitet ist, muss man sich ein klares Bild davon machen, was es physikalisch und chemisch unterscheidet. Das Bis(fluorsulfonyl)imid-Anion – auch FSI⁻ geschrieben – ist ein schwach koordinierendes, stark delokalisiertes Anion, das nur lose mit dem Imidazolium-Kation wechselwirkt. Diese schwache Ionenpaarung ist die Hauptursache für die bemerkenswert niedrige Viskosität der Verbindung im Vergleich zu vielen anderen ionischen Flüssigkeiten. Bei 25 °C hat [EMIM][FSI] eine dynamische Viskosität von ca 18–22 mPa·s , was niedrig genug ist, um eine angemessene Ionenmobilität zu ermöglichen, ohne dass erhöhte Temperaturen erforderlich sind.
Seine Ionenleitfähigkeit liegt bei Raumtemperatur im Bereich von 14–18 mS/cm , einer der höchsten Werte, die jemals für eine reine ionische Flüssigkeit verzeichnet wurden. Dies ist eine direkte Folge der niedrigen Viskosität und der hohen Ladungsdichte des FSI⁻-Anions. Das elektrochemische Fenster – der Spannungsbereich, in dem die Verbindung weder oxidiert noch reduziert wird – liegt je nach Elektrodenmaterial und Messbedingungen bei etwa 4,5 bis 5,5 V. Dieses breite Fenster macht [EMIM][FSI] als Elektrolytmedium für elektrochemische Hochspannungsanwendungen so attraktiv. Sein Schmelzpunkt liegt deutlich unter 0 °C (gemeldete Werte reichen von –18 °C bis –22 °C), was bedeutet, dass es in den meisten Betriebstemperaturbereichen, die für reale Geräte relevant sind, flüssig bleibt.
Elektrolyt in Lithium-Ionen- und Batterien der nächsten Generation
Die kommerziell bedeutendste Anwendung von [EMIM][FSI] ist die Verwendung als Elektrolytkomponente in wiederaufladbaren Batteriesystemen. Herkömmliche Lithium-Ionen-Batterien verwenden organische Carbonatelektrolyte – Ethylencarbonat, Dimethylcarbonat und verwandte Verbindungen – die brennbar sind und bei erhöhten Temperaturen oder nach Missbrauch der Zellen zur Zersetzung neigen. Ionische Flüssigkeiten bieten eine nicht brennbare, thermisch stabile Alternative, und [EMIM][FSI] gehört zu den am besten geeigneten Kandidaten, da seine niedrige Viskosität es Lithiumionen ermöglicht, schnell genug durch den Elektrolyten zu wandern, um praktische Lade- und Entladezyklen zu ermöglichen.
In der Lithiumbatterieforschung wird [EMIM][FSI] typischerweise als Wirtslösungsmittel verwendet, in dem ein Lithiumsalz – am häufigsten Lithium-bis(fluorsulfonyl)imid (LiFSI) – in Konzentrationen zwischen 0,5 M und 3,2 M gelöst wird. Bei hohen Lithiumsalzkonzentrationen bildet der Elektrolyt einen „lokal konzentrierten“ ionischen Flüssigelektrolyten mit verbesserter Kompatibilität mit Graphitanoden, die sonst durch das Imidazoliumkation abgeblättert würden. Studien haben eine stabile Zyklisierung von Graphit/LiFePO₄- und Graphit/NMC-Vollzellen unter Verwendung von [EMIM][FSI]-basierten Elektrolyten bei Temperaturen von –20 °C bis 60 °C gezeigt und Carbonatelektrolyten in beiden Extrembereichen dieses Bereichs überlegen.
Anwendungen für Natriumionen- und Kaliumionenbatterien
Über Lithium hinaus wird [EMIM][FSI] aktiv als Elektrolytmedium für Natriumionen- und Kaliumionenbatterien untersucht – zwei Post-Lithium-Chemikalien, die als kostengünstigere Alternativen für die stationäre Energiespeicherung entwickelt werden. Natrium- und Kaliumsalze des FSI⁻-Anions lösen sich leicht in [EMIM][FSI], und die resultierenden Elektrolyte unterstützen das reversible Plattieren und Ablösen dieser Metalle unter Bedingungen, die in Standardlösungsmitteln auf Carbonat- oder Etherbasis nur schwer zu erreichen sind. Die nicht brennbare Natur des ionischen Flüssigelektrolyten ist besonders attraktiv für großformatige stationäre Speicher, bei denen der Brandschutz eine primäre Designbeschränkung darstellt.
Superkondensatoren und elektrochemische Kondensatorelektrolyte
Elektrochemische Doppelschichtkondensatoren (EDLCs), allgemein Superkondensatoren oder Ultrakondensatoren genannt, speichern Energie durch Adsorption von Ionen an der Oberfläche von Kohlenstoffelektroden mit großer Oberfläche. Die maximal erreichbare Energiedichte in einem EDLC skaliert mit dem Quadrat der Betriebsspannung, was bedeutet, dass die Erweiterung des Spannungsfensters direkt die pro Masseneinheit gespeicherte Energie vervielfacht. Wässrige Elektrolyte begrenzen den EDLC-Betrieb auf etwa 1 V, während organische Elektrolyte ihn auf etwa 2,7 V erhöhen. [EMIM][FSI] ermöglicht mit seinem elektrochemischen Fenster von über 4 V in Kohlenstoffelektrodenzellen den Betrieb von EDLC-Geräten bei 3,5 V oder höher , was die erreichbare Energiedichte im Vergleich zu organischen Elektrolyten auf Acetonitrilbasis nahezu verdoppelt.
Die niedrige Viskosität von [EMIM][FSI] ist in diesem Zusammenhang von entscheidender Bedeutung, da sie es Ionen ermöglicht, effizient in die engen Poren von Aktivkohle- und Karbid-abgeleiteten Kohlenstoffelektrodenmaterialien einzudringen, selbst bei Temperaturen unterhalb der Umgebungstemperatur. Forschungsgruppen haben [EMIM][FSI]-basierte EDLC-Zellen mit spezifischen Energiewerten von mehr als 40 Wh/kg auf Geräteebene demonstriert – ein Maßstab, der sich dem unteren Leistungsbereich von Blei-Säure-Batterien annähert und gleichzeitig die für Kondensatorspeicher charakteristischen Leistungsdichte- und Zykluslebensdauervorteile beibehält.
Galvanische Abscheidung von Metallen und Halbleitern
Die galvanische Abscheidung – der Prozess der Reduktion von Metallionen aus einer Lösung auf einer Elektrodenoberfläche zur Bildung eines dünnen Films oder einer dünnen Beschichtung – ist in wässrigen Elektrolyten stark eingeschränkt, da Wasser unter 1,23 V elektrolysiert. Viele Metalle von industriellem Interesse, darunter Aluminium, Titan, Silizium, Germanium und hochschmelzende Metalle wie Tantal und Niob, können aus Wasser überhaupt nicht galvanisch abgeschieden werden, da ihr Reduktionspotential unterhalb der Wasserstoffentwicklungsgrenze liegt. [EMIM][FSI] löst geeignete Vorläufersalze für mehrere dieser Elemente und bietet das elektrochemische Fenster, das für deren Reduktion ohne konkurrierende Elektrolytzersetzungsreaktionen erforderlich ist.
Die elektrolytische Abscheidung von Aluminium aus [EMIM][FSI]-basierten Elektrolyten, die Aluminiumchlorid (AlCl₃) enthalten, wurde bei Raumtemperatur mit guter Stromeffizienz und kontrollierbarer Filmmorphologie nachgewiesen. Die abgeschiedenen Aluminiumbeschichtungen sind vielversprechend für Korrosionsschutzanwendungen, bei denen herkömmliche wässrige Chromat- oder Nickelbeschichtungen aus Umweltschutzgründen auslaufen. Aus [EMIM][FSI]-basierten Elektrolyten abgeschiedene dünne Silizium- und Germaniumfilme wurden als Anodenmaterialien für Batterieanwendungen untersucht, wobei die Elektroabscheidungsroute eine Alternative zu Hochtemperatur-Vakuumabscheidungsverfahren bietet.
Halbleiter- und Nanostruktursynthese
Die einzigartige Solvatisierungsumgebung von [EMIM][FSI] ermöglicht auch die Synthese von Halbleiter-Nanostrukturen – Quantenpunkte, Nanodrähte und dünne Filme – mit kontrollierter Morphologie und Zusammensetzung. Die ionische Flüssigkeit fungiert gleichzeitig als Lösungsmittel, strukturdirigierendes Mittel und elektrochemisches Medium und steuert die Keimbildung und das Wachstum abgeschiedener Materialien durch ihre organisierte Grenzflächenstruktur an Elektrodenoberflächen. Verbindungshalbleiter wie CdTe und Cu₂ZnSnS₄ (CZTS), die für die Herstellung von Solarzellen relevant sind, wurden aus [EMIM][FSI]-basierten Elektrolyten abgeschieden, wobei die Kontrolle der Zusammensetzung in wässrigen Systemen nicht einfach zu erreichen ist.
Verwendung als Lösungsmittel und Reaktionsmedium in der chemischen Synthese
Ionische Flüssigkeiten werden als „grüne“ Alternativen zu flüchtigen organischen Lösungsmitteln in der chemischen Synthese angepriesen, da ihr vernachlässigbarer Dampfdruck die Lösungsmittelemission während der Reaktionen verhindert. [EMIM][FSI] beteiligt sich an diesem Anwendungsbereich, insbesondere bei Reaktionen, die von seinen spezifischen Solvatisierungseigenschaften profitieren oder bei denen seine elektrochemische Stabilität die Verwendung als kombiniertes Lösungsmittel und Elektrolyt für die Elektrosynthese ermöglicht.
Die organische Elektrosynthese – die Verwendung von Elektrizität anstelle von chemischen Oxidations- oder Reduktionsmitteln, um organische Umwandlungen voranzutreiben – ist ein Bereich von wachsendem industriellem Interesse für die Herstellung pharmazeutischer Zwischenprodukte und Feinchemikalien. [EMIM][FSI] fungiert bei solchen Reaktionen sowohl als Lösungsmittel als auch als Leitelektrolyt, wodurch die Notwendigkeit entfällt, ein separates Salz in einem organischen Lösungsmittel aufzulösen, und die nachgeschaltete Produktisolierung vereinfacht wird. Seine im Vergleich zu anderen ionischen Flüssigkeiten niedrige Viskosität verbessert den Stofftransport innerhalb des elektrochemischen Reaktors, erhöht die Stromeffizienz und verkürzt die Reaktionszeiten.
Bei der elektrochemischen CO₂-Reduktion – einer Reaktion von erheblichem Interesse für die Umwandlung von eingefangenem Kohlendioxid in nützliche Kraftstoffe oder Chemikalien – wurde [EMIM][FSI] als hochwirksames Medium identifiziert. Das Imidazoliumkation beteiligt sich aktiv an der Stabilisierung des CO₂-Radikalanion-Zwischenprodukts, senkt das für die CO₂-Reduktion erforderliche Überpotential und verbessert die Selektivität gegenüber Kohlenmonoxid- oder Formiatprodukten im Vergleich zu wässrigen Elektrolyten.
Schmierung und tribologische Anwendungen
Die thermische Stabilität, Nichtflüchtigkeit und einstellbare Oberflächenaffinität von [EMIM][FSI] machen es zu einem brauchbaren Schmierstoffadditiv und reinen Schmierstoff für anspruchsvolle tribologische Anwendungen. Im Gegensatz zu Schmiermitteln auf Erdölbasis verdunstet es unter Vakuumbedingungen nicht und eignet sich daher für den Einsatz in Raumfahrtmechanismen, Vakuumkammern und Lagern von Präzisionsinstrumenten, bei denen die Ausgasung minimiert werden muss. Studien mit [EMIM][FSI] als Schmiermittel bei Stahl-auf-Stahl-Gleitkontakten haben eine deutliche Verringerung des Reibungskoeffizienten und des Verschleißvolumens im Vergleich zu ungeschmierten Oberflächen und zu Referenz-Mineralölschmiermitteln gezeigt.
Das FSI⁻-Anion trägt zur tribologischen Leistung bei, indem es unter Scherbedingungen einen schützenden Tribofilm auf Metalloberflächen bildet. Der Fluorgehalt des Anions spielt eine analoge Rolle wie der von PTFE-Partikeln (Polytetrafluorethylen) in herkömmlichen Schmierstoffformulierungen und sorgt für eine niederenergetische Oberflächenchemie, die den Klebstoffverschleiß reduziert. Für Aluminiumlegierungen und Weichmetalle, die sich nur schwer mit Schwefel-Phosphor-Additivchemie schützen lassen (die Nichteisenoberflächen angreifen können), bietet [EMIM][FSI] eine chemisch verträgliche Alternative.
Zusammenfassung der wichtigsten Anwendungsbereiche
Die folgende Tabelle fasst die Hauptverwendungen von [EMIM][FSI] zusammen mit der spezifischen Eigenschaft zusammen, die es für jeden Anwendungsbereich geeignet macht.
| Bewerbung | Wichtige genutzte Eigenschaft | Leistungshighlight |
|---|---|---|
| Li/Na/K-Ionen-Batterieelektrolyt | Hohe Ionenleitfähigkeit, nicht brennbar | Stabiler Zyklenbetrieb von −20 °C bis 60 °C |
| Superkondensator-Elektrolyt | Breites elektrochemisches Fenster, niedrige Viskosität | Betriebsspannung >3,5 V; Energiedichte >40 Wh/kg |
| Elektroabscheidung von Metallen und Halbleitern | Breites elektrochemisches Fenster, vernachlässigbares Wasser | Ermöglicht die Abscheidung von Al, Si und Ge bei Raumtemperatur |
| Elektrosynthese und CO₂-Reduktion | Kationenvermittelte Zwischenstabilisierung | Reduziertes Überpotential; verbesserte CO-Selektivität |
| Schmierung (Vakuum-/Präzisionssysteme) | Null Dampfdruck, thermische Stabilität | Im Vakuum lebensfähig; schützender, von FSI abgeleiteter Tribofilm |
Handhabung, Sicherheit und praktische Überlegungen
Obwohl [EMIM][FSI] weitaus weniger gefährlich ist als die flüchtigen organischen Lösungsmittel, die es oft ersetzt, ist es nicht ohne Anforderungen an die Handhabung. Die Verbindung ist hygroskopisch – sie absorbiert Wasser aus der Umgebungsluft – und gelöstes Wasser beeinflusst ihr elektrochemisches Fenster, ihre Viskosität und ihre Leitfähigkeit. Für elektrochemische Anwendungen, die eine Leistung an den Grenzen des Stabilitätsfensters erfordern, sollte [EMIM][FSI] unter Vakuum bei 60–80 °C und Rühren getrocknet werden, bis der Wassergehalt darunter liegt 20 ppm gemessen durch Karl-Fischer-Titration.
- In verschlossenen Behältern unter inerter Atmosphäre (Argon oder Stickstoff) lagern, um die Feuchtigkeitsaufnahme zu minimieren und jegliche Reaktion mit atmosphärischem CO₂ zu verhindern, das die Zusammensetzung der ionischen Flüssigkeit über längere Zeiträume verändern kann.
- Vermeiden Sie längeren Hautkontakt – während [EMIM][FSI] eine geringe akute Toxizität aufweist, zeigen ionische Flüssigkeiten als Klasse biologische Aktivität auf zellulärer Ebene und kumulative Expositionsdaten werden immer noch von Arbeitsschutzforschern gesammelt.
- Behandeln Sie Glaswaren und Geräte, die mit [EMIM][FSI] verwendet werden, vorsichtig – seine niedrige Oberflächenspannung bedeutet, dass es Oberflächen aggressiv benetzt und sich ohne gründliches Waschen mit Lösungsmittel nur schwer vollständig von porösen oder aufgerauten Oberflächen entfernen lässt.
- Die Entsorgung sollte gemäß den örtlichen Vorschriften für fluorhaltige Chemikalien erfolgen – das FSI⁻-Anion enthält Fluorsulfonylgruppen, die bei der Verbrennung fluoridhaltige Nebenprodukte erzeugen und nicht ohne entsprechende Behandlung in normalen wässrigen Abfallströmen entsorgt werden sollten.
Da die Forschung zu ionischen Flüssigkeiten immer ausgereifter wird und die Möglichkeiten zur Maßstabsvergrößerung für die [EMIM][FSI]-Produktion immer kostengünstiger werden, schließt sich die Lücke zwischen Laborleistung und kommerziellem Einsatz stetig. Seine Kombination aus elektrochemischer Breite, niedriger Viskosität und thermischer Robustheit macht es zu einer der technisch am besten geeigneten ionischen Flüssigkeiten für den Übergang von der akademischen Forschung in die industrielle Praxis in mehreren Sektoren.


 English
English Deutsch
Deutsch Español
Español 中文简体
中文简体