Content
- 1 Was ist N-Methylimidazoliumhydrogensulfat?
- 2 Chemische Identität und strukturelle Eigenschaften
- 3 Wichtige physikalische und chemische Eigenschaften
- 4 Rolle als Säurekatalysator in der organischen Synthese
- 5 Biomasseverarbeitung und Zelluloseauflösung
- 6 Biodieselsynthese und Veresterungskatalyse
- 7 Elektrochemische Anwendungen und Protonenleitung
- 8 Handhabung, Sicherheit und Umweltaspekte
- 9 Zusammenfassung der Hauptverwendungen
Was ist N-Methylimidazoliumhydrogensulfat?
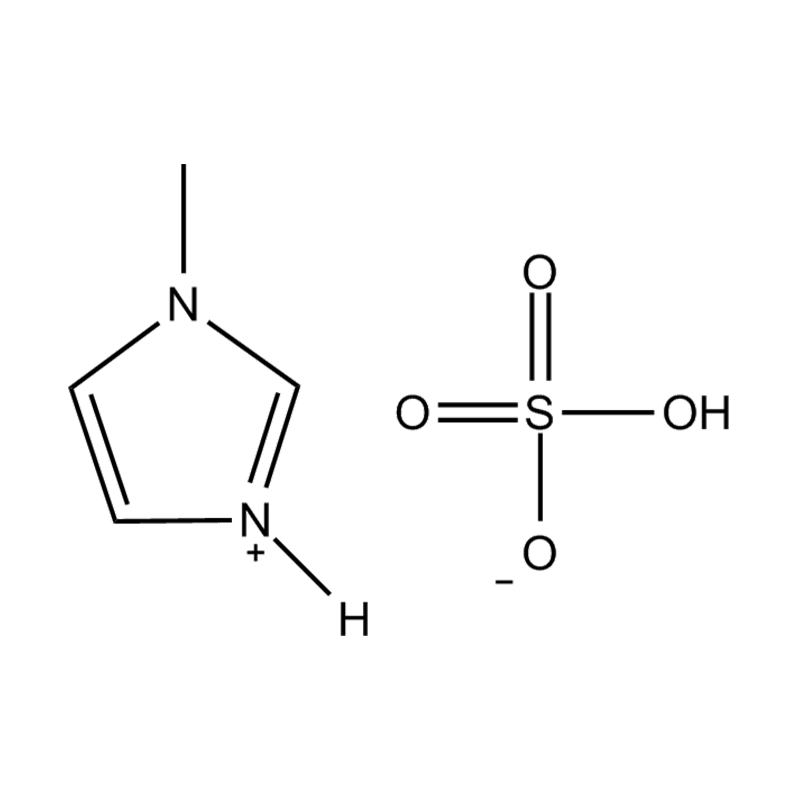
N-Methylimidazoliumhydrogensulfat , allgemein geschrieben als [Hmim][HSO₄], ist eine Brønsted-saure ionische Flüssigkeit, die durch Protonierung von 1-Methylimidazol mit Schwefelsäure entsteht. Im Gegensatz zu herkömmlichen ionischen Flüssigkeiten, die typischerweise durch Quaternisierungsreaktionen gebildet werden, behält diese Verbindung ein saures Proton am Imidazoliumstickstoff, was ihr eine einzigartige Kombination aus ionischen Flüssigkeitseigenschaften und starker Brønsted-Säure-Funktionalität verleiht. Es gehört zur größeren Familie der protischen ionischen Flüssigkeiten (PILs), die sich von aprotischen ionischen Flüssigkeiten durch das Vorhandensein eines übertragbaren Protons und das damit verbundene Wasserstoffbrückennetzwerk, das dadurch innerhalb der Flüssigkeitsstruktur entsteht, unterscheiden.
Die Verbindung hat in den letzten zwei Jahrzehnten großes Forschungs- und Industrieinteresse geweckt, da sie gleichzeitig als Lösungsmittel, Katalysator und Reaktionsmedium fungiert – Aufgaben, die in der konventionellen Chemie typischerweise auf mehrere separate Reagenzien verteilt sind. Seine Synthese ist unkompliziert und skalierbar, sein Toxizitätsprofil ist im Allgemeinen günstiger als bei vielen herkömmlichen Säurekatalysatoren und sein vernachlässigbarer Dampfdruck minimiert die Exposition der Arbeiter und die Emissionen in die Atmosphäre. Diese Eigenschaften haben [Hmim][HSO₄] zu einem Gegenstand intensiver Forschung in den Bereichen grüne Chemie, Biomasseumwandlung, Elektrochemie und organische Synthese gemacht.
Chemische Identität und strukturelle Eigenschaften
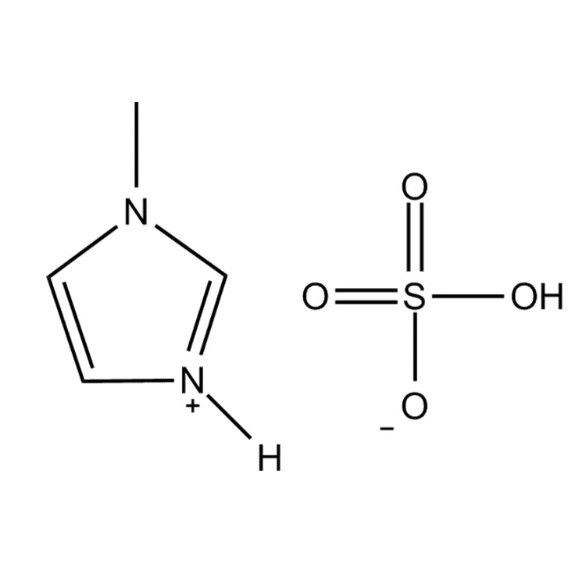
Die Molekülstruktur von N-Methylimidazoliumhydrogensulfat besteht aus einem 1-Methylimidazolium-Kation ([Hmim]⁺), gepaart mit einem Hydrogensulfat-Anion ([HSO₄]⁻). Das Kation entsteht, wenn der N-3-Stickstoff von 1-Methylimidazol ein Proton aus Schwefelsäure aufnimmt, wodurch ein positiv geladener aromatischer Ring mit einer Methylgruppe an N-1 und einem Proton an N-3 entsteht. Das Hydrogensulfat-Anion behält einen sauren Wasserstoff und ist dadurch in der Lage, sowohl Wasserstoffbrückenbindungen abzugeben als auch aufzunehmen, was die physikalischen Eigenschaften des Materials erheblich beeinflusst.
Diese Wasserstoffbindung zwischen der N-H-Gruppe des Kations und den Sauerstoffatomen des Anions erzeugt ein ausgedehntes ionisches Netzwerk, das den Schmelzpunkt im Vergleich zu vielen ionischen Flüssigkeiten auf Imidazoliumbasis erhöht und zur relativ hohen Viskosität der Verbindung bei Raumtemperatur beiträgt. Der Imidazoliumring selbst ist planar und aromatisch und trägt zu π-π-Stapelwechselwirkungen bei, die die flüssige Phase auf molekularer Ebene weiter strukturieren. Das Verständnis dieser Strukturmerkmale ist wichtig, um vorherzusagen, wie sich die Verbindung in verschiedenen Lösungsmittelsystemen und bei verschiedenen Temperaturen verhält.
Wichtige physikalische und chemische Eigenschaften
Die physikalischen und chemischen Eigenschaften von [Hmim][HSO₄] sind für seinen praktischen Nutzen direkt relevant. Die folgende Tabelle fasst die wichtigsten dokumentierten Werte zusammen:
| Eigentum | Gemeldeter Wert/Beschreibung |
| Molekulare Formel | C₄H₇N₂⁺ · HSO₄⁻ (C₄H₈N₂O₄S) |
| Molekulargewicht | ~180,18 g/mol |
| Aussehen | Farblose bis hellgelbe viskose Flüssigkeit oder Feststoff |
| Schmelzpunkt | ~29–35°C (variiert je nach Reinheit und Wassergehalt) |
| Zersetzungstemperatur | >200°C (thermisch stabil bis ~220°C) |
| Dampfdruck | Bei Umgebungsbedingungen vernachlässigbar |
| Viskosität (bei 25°C) | Relativ hoch; nimmt mit der Temperatur deutlich ab |
| Löslichkeit in Wasser | Vollständig mischbar; stark hygroskopisch |
| Säure | Starke Brønsted-Säure; Anwendbare Hammett-Säurefunktion |
| Elektrische Leitfähigkeit | Mäßig bis hoch; geeignet für elektrochemische Anwendungen |
| Polarität | Hohe Polarität; löst polare und einige unpolare Substrate |
Thermische Stabilität und Flüssigkeitsbereich
Die thermische Stabilität von [Hmim][HSO₄] ist eine seiner betrieblich wertvollsten Eigenschaften. Studien zur thermogravimetrischen Analyse (TGA) zeigen, dass sich die Verbindung bei Temperaturen über etwa 200 bis 220 °C zu zersetzen beginnt, was ihr ein breites Betriebsfenster in der flüssigen Phase gibt, sobald sie nahe Raumtemperatur schmilzt. Dieser breite Temperaturbereich ist weitaus größer als bei den meisten herkömmlichen molekularen Lösungsmitteln und ermöglicht die Durchführung von Reaktionen bei erhöhten Temperaturen ohne das Risiko einer Lösungsmittelverdampfung, Rückflussverlusten oder eines Druckaufbaus in geschlossenen Systemen. Aufgrund des niedrigen Schmelzpunkts nahe der Umgebungstemperatur kann es in den meisten Labor- und Industrieumgebungen ohne Vorheizen als Flüssigkeit gehandhabt werden.
Brønsted-Azidität und Protonentransferverhalten
Die bestimmende chemische Eigenschaft von [Hmim][HSO₄] ist seine starke Brønsted-Acidität, die sowohl vom N-H-Proton am Imidazolium-Kation als auch vom sauren Proton des Hydrogensulfat-Anions herrührt. Diese Dual-Source-Acidität verleiht der Verbindung eine höhere effektive Protonenverfügbarkeit im Vergleich zu ionischen Flüssigkeiten auf der Basis monoprotonischer Säuren. Die für diese Verbindung und verwandte Systeme gemessenen Werte der Hammett-Säurefunktion (H₀) bestätigen Säurewerte, die für protonenkatalysierte Reaktionen wirksam sind, ohne dass der Supersäurebereich erreicht wird. Dies macht [Hmim][HSO₄] zu einem kontrollierbaren und selektiven Säurekatalysator, der Reaktionen fördern kann, die eine erhebliche Protonenaktivität erfordern, ohne die unkontrollierte Reaktivität und Korrosivität, die mit konzentrierten Mineralsäuren verbunden sind.
Rolle als Säurekatalysator in der organischen Synthese
Die am umfassendsten untersuchte Anwendung von N-Methylimidazoliumhydrogensulfat ist die Verwendung als Brønsted-Säure-Katalysator für organische Reaktionen. In dieser Funktion ersetzt es herkömmliche flüssige Säuren wie Schwefelsäure, Salzsäure und p-Toluolsulfonsäure und bietet gleichzeitig die zusätzlichen Vorteile der Recyclingfähigkeit, der geringen Flüchtigkeit und der einfacheren Produkttrennung. Die Phase der ionischen Flüssigkeit und die Phase des organischen Produkts trennen sich nach Abschluss der Reaktion häufig spontan, sodass der Katalysator durch einfaches Dekantieren zurückgewonnen und über mehrere Reaktionszyklen hinweg mit minimalem Aktivitätsverlust wiederverwendet werden kann.
Zu den wichtigsten Reaktionstypen, die durch [Hmim][HSO₄] effektiv katalysiert werden, gehören Veresterung und Umesterung, Fischer-Indolsynthese, Beckmann-Umlagerung, Fries-Umlagerung, Friedel-Crafts-Acylierung unter milden Bedingungen und die Synthese heterozyklischer Verbindungen einschließlich Dihydropyrimidinonen über die Biginelli-Reaktion. Bei Veresterungsreaktionen zeigte die Verbindung eine katalytische Aktivität, die mit konzentrierter Schwefelsäure bei äquivalenten Säurebeladungen vergleichbar war, während gleichzeitig weniger Nebenprodukte gebildet wurden und eine einfache Aufarbeitung möglich war. Seine Fähigkeit, gleichzeitig als Lösungsmittel und Katalysator zu fungieren – in einem sogenannten „Lösungsmittel-Katalysator“-System – ist besonders attraktiv, da dadurch die Notwendigkeit eines zusätzlichen inerten Lösungsmittels entfällt, wodurch die Prozesskomplexität und die Abfallerzeugung reduziert werden.
Biomasseverarbeitung und Zelluloseauflösung
Zu den einflussreichsten neuen Anwendungen von [Hmim][HSO₄] gehört seine Verwendung bei der Vorbehandlung und chemischen Umwandlung von Lignozellulose-Biomasse. Die Umwandlung landwirtschaftlicher Abfälle, Holz und Energiepflanzen in fermentierbare Zucker, Plattformchemikalien und Biokraftstoffe erfordert den Abbau der äußerst widerspenstigen Zellulose- und Hemizellulosematrix – eine Herausforderung, die in der Vergangenheit entweder teure Enzymcocktails oder aggressive chemische Behandlungen erforderte. Brønsted-saure ionische Flüssigkeiten auf Basis des Hydrogensulfat-Anions haben gezeigt, dass sie in der Lage sind, Wasserstoffbrückenbindungsnetzwerke in Cellulose aufzubrechen und so deren Auflösung, Hydrolyse und anschließende Umwandlung unter relativ milden Bedingungen zu erleichtern.
Forschungsgruppen haben gezeigt, dass [Hmim][HSO₄] und verwandte saure ionische Flüssigkeiten unter optimierten Mikrowellen- oder thermisch unterstützten Bedingungen Cellulose mit Ausbeuten von über 50 bis 70 Prozent zu Glucose hydrolysieren können und damit die Hydrolyse mit verdünnter Säure unter gleichwertigen Bedingungen deutlich übertreffen. Die ionische Flüssigkeitsphase kann auch Hemizellulose selektiv auflösen, während Lignin weitgehend intakt bleibt, was Fraktionierungsstrategien ermöglicht, die jede Biomassekomponente separat aufwerten. Die Recyclingfähigkeit der ionischen Flüssigkeitsphase ist ein entscheidender wirtschaftlicher Vorteil bei der Biomasseverarbeitung, da sie die höheren Anfangskosten der ionischen Flüssigkeitssynthese im Vergleich zu Mineralsäurekatalysatoren ausgleicht.
Biodieselsynthese und Veresterungskatalyse
Die Herstellung von Biodiesel durch säurekatalysierte Veresterung freier Fettsäuren (FFAs) ist ein spezifischer Bereich, in dem [Hmim][HSO₄] großes kommerzielles Interesse geweckt hat. Herkömmliche basenkatalysierte Biodieselprozesse reagieren sehr empfindlich auf den FFA-Gehalt des Ausgangsmaterials. Wenn der FFA-Gehalt etwa 2 Prozent übersteigt, wird das Verfahren durch Seifenbildung und Katalysatordeaktivierung unwirtschaftlich. Säurekatalysatoren können mit Ausgangsmaterialien mit hohem FFA-Gehalt umgehen, herkömmliche flüssige Säuren verursachen jedoch Korrosionsprobleme, erfordern wässrige Aufarbeitungsschritte, die Abwasser erzeugen, und können nicht einfach zurückgewonnen werden.
[Hmim][HSO₄] löst diese Probleme, indem es eine starke Brønsted-Acidität in einem nicht korrosiven, rückgewinnbaren Flüssigkatalysatorformat bereitstellt. Mehrere Studien haben FFA-Umwandlungsraten von über 90 Prozent bei Verwendung dieser ionischen Flüssigkeit unter moderaten Bedingungen (60–80 °C, atmosphärischer Druck) gemeldet, wobei das Katalysatorrecycling über fünf oder mehr Zyklen ohne nennenswerten Aktivitätsverlust nachgewiesen wurde, wenn es zwischen den Anwendungen ordnungsgemäß getrocknet wurde. Die Phasentrennung zwischen der Methanol-Ester-Glycerin-Produktphase und der ionischen Flüssigkeitsphase erleichtert die Produktrückgewinnung ohne wässrige Waschschritte und macht den Prozess deutlich sauberer als herkömmliche säurekatalysierte Veresterungswege.
Elektrochemische Anwendungen und Protonenleitung
Die Ionenleitfähigkeit und die Protonenübertragungseigenschaften von [Hmim][HSO₄] machen es zu einem geeigneten Elektrolytmaterial für elektrochemische Geräte, insbesondere Protonenaustauschmembran-Brennstoffzellen (PEMFCs), die bei mittleren Temperaturen (100–200 °C) betrieben werden. Herkömmliche Nafion-basierte Membranen in PEMFCs erfordern eine kontinuierliche Befeuchtung und funktionieren über 80 °C schlecht, was zu technischen Herausforderungen für das Wärmemanagement und die Katalysatortoleranz führt. Protische ionische Flüssigkeiten, die auf dem Imidazolium-Hydrogensulfat-System basieren, zeigen Protonenleitfähigkeit durch einen Grotthuss-Mechanismus, bei dem Protonen entlang des wasserstoffgebundenen Ionennetzwerks hüpfen, das bei Temperaturen deutlich über 100 °C ohne Verwendung von flüssigem Wasser aktiv bleibt.
Untersuchungen an Verbundmembranen mit [Hmim][HSO₄] in Polymermatrizen haben Leitfähigkeitswerte im Bereich von 10⁻³ bis 10⁻² S/cm bei Temperaturen zwischen 100 und 180 °C ergeben – vergleichbar mit befeuchtetem Nafion im gleichen Temperaturbereich. Dies eröffnet Möglichkeiten für den wasserfreien oder feuchtigkeitsarmen PEMFC-Betrieb, was das Systemdesign vereinfachen und die Toleranz gegenüber CO-Vergiftung von Platinkatalysatoren verbessern würde. Über Brennstoffzellen hinaus machen die Leitfähigkeit und das breite elektrochemische Fenster der Verbindung sie auch für den Einsatz in Superkondensatorelektrolyten und Elektroabscheidungsmedien attraktiv.
Handhabung, Sicherheit und Umweltaspekte
Während ionische Flüssigkeiten aufgrund ihrer vernachlässigbaren Flüchtigkeit häufig als „grüne“ Lösungsmittel beschrieben werden, muss das Umwelt- und Sicherheitsprofil von [Hmim][HSO₄] im gesamten Kontext bewertet werden. Die Verbindung ist stark sauer und wirkt ätzend auf Haut und Schleimhäute. Bei der Handhabung ist daher geeignete persönliche Schutzausrüstung einschließlich chemikalienbeständiger Handschuhe, Augenschutz und ausreichender Belüftung erforderlich. Aufgrund seiner hohen Hygroskopizität muss der Wassergehalt bei Anwendungen, bei denen wasserfreie Bedingungen erforderlich sind, sorgfältig kontrolliert werden, da absorbierte Feuchtigkeit die Viskosität, den Schmelzpunkt und die katalytische Aktivität erheblich verändern kann.
Aus ökologischer Sicht wurde gezeigt, dass [Hmim][HSO₄] und strukturell verwandte ionische Imidazoliumflüssigkeiten in höheren Konzentrationen eine aquatische Toxizität gegenüber bestimmten Mikroorganismen aufweisen und der biologische Abbau in herkömmlichen Abwasserbehandlungssystemen langsam ist. Eine verantwortungsvolle Nutzung erfordert die Eindämmung von Prozessströmen, die Vermeidung von Einleitungen in Gewässer und die Umsetzung von Rückgewinnungs- und Recyclingprotokollen, die die Wiederverwendung maximieren und die Entsorgung minimieren. Die Entwicklung biologisch abbaubarer Analoga ionischer Flüssigkeiten mit biobasierten Anionen oder Kationen ist eine aktive Forschungsrichtung, die darauf abzielt, diese Bedenken auszuräumen und gleichzeitig die funktionellen Vorteile der Verbindungsklasse zu bewahren.
Zusammenfassung der Hauptverwendungen
Die Vielseitigkeit von N-Methylimidazoliumhydrogensulfat in verschiedenen Anwendungsbereichen spiegelt seine Kombination aus starker Brønsted-Säure, ionischen Flüssigkeitseigenschaften, thermischer Stabilität und Recyclingfähigkeit wider. Zu den wichtigsten in der Literatur und in der industriellen Praxis dokumentierten Anwendungen gehören:
- Säurekatalysator für die Veresterung und Biodieselproduktion aus Rohstoffen mit hohem FFA-Gehalt mit einfacher Phasentrennung und Katalysatorrückgewinnung.
- Lösungsmittelkatalysator für die organische Synthese einschließlich Biginelli-Reaktionen, Fischer-Indolsynthese und Friedel-Crafts-Umwandlungen ohne zusätzliches Lösungsmittel.
- Biomassevorbehandlung und Cellulosehydrolyse zur Herstellung von fermentierbaren Zuckern und Plattformchemikalien aus Lignozellulose-Rohstoffen.
- Elektrolytkomponente in Mitteltemperatur-Brennstoffzellen und elektrochemische Geräte, die eine wasserfreie Protonenleitung über 100 °C erfordern.
- Reaktionsmedium für die Heterocyclensynthese wo die saure ionische Flüssigkeitsumgebung Zyklisierungs- und Kondensationsreaktionen mit verbesserter Selektivität fördert.
- Extraktionsmittel und Phasentransfermedium in der Trennchemie, insbesondere zur Extraktion polarer Verbindungen aus wässrigen Systemen oder zur Erleichterung von zweiphasigen Flüssig-Flüssig-Reaktionen.
Während die Forschung in der Chemie ionischer Flüssigkeiten immer weiter voranschreitet, bleibt [Hmim][HSO₄] aufgrund seiner zugänglichen Synthese, gut charakterisierten Eigenschaften und nachgewiesenen Leistung in einem einzigartig breiten Spektrum chemischer und elektrochemischer Anwendungen eines der am häufigsten untersuchten und praktisch eingesetzten Mitglieder der Familie der Brønsted-sauren ionischen Flüssigkeiten.


 English
English Deutsch
Deutsch Español
Español 中文简体
中文简体