Content
- 1 Was ist 1-Ethyl-3-methylimidazoliumtrifluormethansulfonat?
- 2 Wichtige physikalische und chemische Eigenschaften
- 3 Synthese- und Reinigungsmethoden
- 4 Elektrochemische Anwendungen: Elektrolyte und Energiespeicherung
- 5 Katalyse- und organische Syntheseanwendungen
- 6 Anwendungen in der Materialwissenschaft und Nanotechnologie
- 7 Sicherheits-, Handhabungs- und Umweltaspekte
- 8 Auswahl von [EMIM][OTf] für Ihre Anwendung: Wichtige Entscheidungskriterien
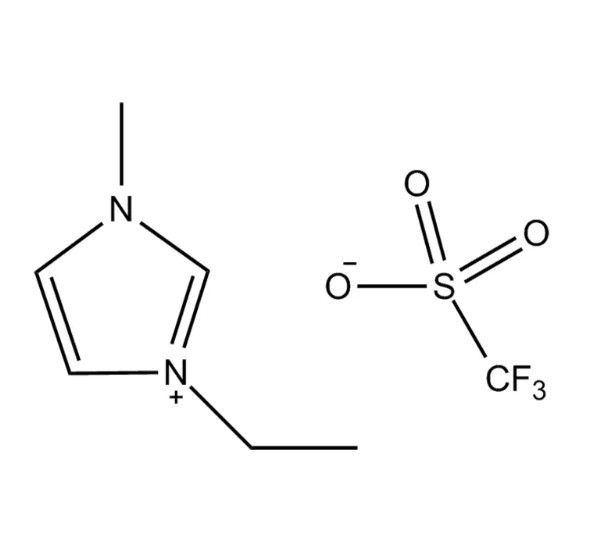
Was ist 1-Ethyl-3-methylimidazoliumtrifluormethansulfonat?
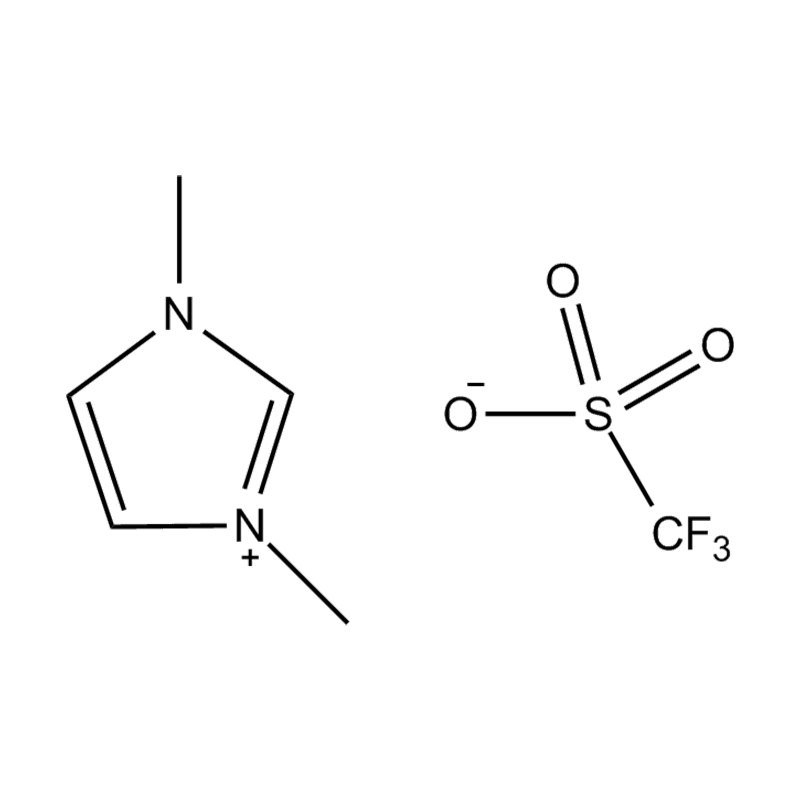
1-Ethyl-3-methylimidazoliumtrifluormethansulfonat , allgemein als [EMIM][OTf] oder EMIMOTf abgekürzt, ist eine ionische Flüssigkeit bei Raumtemperatur (RTIL) aus der Imidazoliumfamilie – einer der am umfassendsten untersuchten und kommerziell bedeutendsten Klassen ionischer Flüssigkeiten in der modernen Chemie. Sein IUPAC-Name spiegelt seine Zwei-Ionen-Architektur wider: ein 1-Ethyl-3-methylimidazolium-Kation gepaart mit einem Trifluormethansulfonat-Anion (Triflat). Die Verbindung trägt die CAS-Registrierungsnummer 145022-44-2 und hat die Summenformel C₇H₁₁F₃N₂O₃S mit einem Molekulargewicht von etwa 260,23 g/mol. Im Gegensatz zu herkömmlichen organischen Lösungsmitteln liegt [EMIM][OTf] bei oder nahe Raumtemperatur als Flüssigkeit vor, obwohl es vollständig aus Ionen besteht. Diese Eigenschaft unterscheidet ionische Flüssigkeiten sowohl von herkömmlichen Salzschmelzen als auch von molekularen Lösungsmitteln und unterstreicht ihre bemerkenswerte Vielseitigkeit als funktionelle Materialien.
Das Triflatanion (CF₃SO₃⁻) ist ein schwach koordinierendes, hochstabiles Anion, das der ionischen Flüssigkeit besondere physikalisch-chemische Eigenschaften verleiht – darunter niedrige Viskosität im Vergleich zu vielen anderen Imidazoliumsalzen, breite elektrochemische Stabilität, ausgezeichnete thermische Beständigkeit und hohe Ionenleitfähigkeit. Diese Eigenschaften haben ein erhebliches akademisches und industrielles Interesse an [EMIM][OTf] als Lösungsmittel, Elektrolyt, Katalysatormedium und Funktionsmaterial in allen Disziplinen geweckt, die von Elektrochemie und Materialwissenschaften bis hin zu pharmazeutischer Synthese und grüner Chemie reichen.
Wichtige physikalische und chemische Eigenschaften
Das Verständnis der spezifischen physikalisch-chemischen Eigenschaften von [EMIM][OTf] ist für die Beurteilung seiner Eignung für eine bestimmte Anwendung von entscheidender Bedeutung. Die Eigenschaften der Verbindung sind in der wissenschaftlichen Literatur gut beschrieben und stellen eine günstige Kombination aus Stabilität, Leitfähigkeit und Verarbeitbarkeit dar, die sie von vielen konkurrierenden ionischen Flüssigkeiten unterscheidet.
| Eigentum | Wert/Beschreibung |
| Molekulare Formel | C₇H₁₁F₃N₂O₃S |
| Molekulargewicht | 260,23 g/mol |
| Schmelzpunkt | ~ -9°C (flüssig bei Raumtemperatur) |
| Thermische Zersetzungstemperatur | > 400°C |
| Viskosität (25°C) | ~ 43–45 mPa·s |
| Ionenleitfähigkeit (25°C) | ~ 8–9 mS/cm |
| Elektrochemisches Fenster | ~ 4,1–4,3 V |
| Dampfdruck | Bei Umgebungsbedingungen vernachlässigbar |
| Aussehen | Farblose bis hellgelbe Flüssigkeit |
| Löslichkeit in Wasser | Mischbar |
Der vernachlässigbare Dampfdruck von [EMIM][OTf] ist eine seiner praktisch bedeutsamsten Eigenschaften. Herkömmliche organische Lösungsmittel wie Acetonitril, Dichlormethan und Diethylether verdampfen bei Umgebungsbedingungen leicht und erzeugen Emissionen flüchtiger organischer Verbindungen (VOC), die Gesundheitsrisiken, Brandgefahren und Umweltprobleme mit sich bringen. Da [EMIM][OTf] unter normalen Betriebsbedingungen praktisch keinen Dampfdruck ausübt, verdunstet es nicht, wodurch Lösungsmittelverluste während der Reaktionen vermieden werden, die Produktisolierung durch Verdampfung vereinfacht wird und das Risiko einer Luftbelastung in Labor- und Industrieumgebungen drastisch reduziert wird.
Synthese- und Reinigungsmethoden
Die Synthese von [EMIM][OTf] ist im Vergleich zu vielen Spezialchemikalien unkompliziert und kann durch etablierte Metathese- und direkte Alkylierungswege erreicht werden. Der direkteste Syntheseweg beinhaltet die Quaternisierung von 1-Methylimidazol mit Ethyltrifluormethansulfonat (Ethyltriflat) in einer einstufigen Reaktion. Wenn 1-Methylimidazol mit Ethyltriflat – einem hochreaktiven Alkylierungsmittel – kombiniert wird, wird das Stickstoffatom an der 3-Position des Imidazolrings einer N-Alkylierung unterzogen, wodurch direkt die ionische Flüssigkeit [EMIM][OTf] entsteht, ohne dass ein Anionenaustauschschritt erforderlich ist.
Ein alternativer zweistufiger Weg stellt zunächst 1-Ethyl-3-methylimidazoliumhalogenid (typischerweise das Chlorid- oder Bromidsalz) her, indem 1-Methylimidazol mit einem Ethylhalogenid umgesetzt wird, und führt dann eine Anionenaustauschreaktion durch, indem das Halogenidsalz mit einer Silbertriflat-, Lithiumtriflat- oder Trifluormethansulfonsäurelösung behandelt wird, um das Halogenidanion durch das Triflatanion zu ersetzen. Während dieser Weg den Einsatz des gefährlichen Ethyltriflat-Reagens vermeidet, bringt er die Herausforderung mit sich, restliche Halogenidverunreinigungen zu entfernen, die für elektrochemische Anwendungen, bei denen Halogenidverunreinigungen zu erheblichen Leistungseinbußen führen, auf Werte im Sub-ppm-Bereich reduziert werden müssen.
Die Reinigung von [EMIM][OTf] umfasst typischerweise die folgenden Schritte, um eine Reinheit in Forschungs- oder Anwendungsqualität sicherzustellen:
- Waschen mit Aktivkohle in Acetonitrillösung, um farbige organische Verunreinigungen und Spuren von Ausgangsmaterialien zu entfernen
- Filtration durch neutrale Aluminiumoxid- oder Kieselgelsäulen zur Entfernung polarer Verunreinigungen und restlicher Metallionen
- Rotationsverdampfung unter reduziertem Druck zur Entfernung flüchtiger Lösungsmittel, die in den Reinigungsschritten verwendet werden
- Trocknen unter Hochvakuum bei erhöhter Temperatur (normalerweise 60–80 °C für 24–48 Stunden), um den Wassergehalt für feuchtigkeitsempfindliche Anwendungen auf unter 20 ppm zu reduzieren
- Überprüfung des Halogenidgehalts durch Ionenchromatographie oder Silbernitrattitration, um die Entfernung unterhalb des anwendungsspezifischen Schwellenwerts zu bestätigen
Das Management des Wassergehalts ist besonders wichtig für [EMIM][OTf], das für elektrochemische Zwecke bestimmt ist, da absorbierte Feuchtigkeit das elektrochemische Fenster erheblich verringert, die Leitfähigkeit durch Protonentransportmechanismen erhöht, die Leistungsdaten verzerren, und empfindliche Elektrodenmaterialien oder gelöste Spezies hydrolysieren kann. Getrocknetes [EMIM][OTf] sollte unter Inertatmosphäre (Argon oder Stickstoff) in verschlossenen Behältern gelagert werden, um eine erneute Aufnahme von Luftfeuchtigkeit zu verhindern.
Elektrochemische Anwendungen: Elektrolyte und Energiespeicherung
Die elektrochemischen Eigenschaften von [EMIM][OTf] machen es zu einem der am aktivsten erforschten ionischen Flüssigkeitselektrolyten für fortschrittliche Energiespeicher- und -umwandlungsgeräte. Seine Kombination aus breitem elektrochemischem Stabilitätsfenster (~4,1–4,3 V), hoher Ionenleitfähigkeit (~8–9 mS/cm bei Raumtemperatur), vernachlässigbarer Flüchtigkeit und thermischer Stabilität bis über 400 °C beseitigt mehrere grundlegende Einschränkungen herkömmlicher Elektrolyte auf Basis organischer Carbonatlösungsmittel, die brennbar und flüchtig sind und in der Praxis auf elektrochemische Fenster von etwa 4–5 V beschränkt sind.
Superkondensatoren und elektrische Doppelschichtkondensatoren
In elektrischen Doppelschichtkondensatoren (EDLCs) beruht der Energiespeichermechanismus auf der elektrostatischen Ionenadsorption an der Grenzfläche zwischen Elektrode und Elektrolyt und nicht auf faradayschen chemischen Reaktionen. [EMIM][OTf] wurde aufgrund seiner günstigen Ionengröße, die ein effektives Eindringen in die mikroporöse Struktur von Aktivkohleelektroden ermöglicht, und seines breiten elektrochemischen Fensters, das den Betrieb bei höheren Zellspannungen als bei wässrigen Elektrolyten ermöglicht, ausführlich als EDLC-Elektrolyt untersucht. Eine höhere Betriebsspannung erhöht direkt die Energiedichte (die mit dem Quadrat der Spannung skaliert), wodurch ionische Flüssigkeitselektrolyte wie [EMIM][OTf] für die Entwicklung von Superkondensatoren mit hoher Energiedichte der nächsten Generation von zentraler Bedeutung sind. Forschungsgruppen haben gezeigt, dass [EMIM][OTf]-basierte EDLCs bei Zellspannungen von 3,5 V oder mehr stabil arbeiten, verglichen mit der Grenze von 1,0–1,2 V in wässrigen Systemen.
Lithium-Ionen- und Natrium-Ionen-Batterieelektrolyte
Mischungen von [EMIM][OTf] mit Lithiumtriflat oder Natriumtriflat wurden als sicherere Alternativen zu herkömmlichen brennbaren Carbonatelektrolyten in Lithium-Ionen- und Natrium-Ionen-Batterien untersucht. Die Nichtentflammbarkeit und thermische Stabilität von [EMIM][OTf]-basierten Elektrolyten trägt direkt dem Sicherheitsrisiko durch thermisches Durchgehen Rechnung, das der Batteriesicherheit in Elektrofahrzeuganwendungen große Aufmerksamkeit geschenkt hat. Herausforderungen bestehen weiterhin bei der Optimierung der Festelektrolyt-Interphase (SEI), die auf Lithiummetall- und Graphitanoden in ionischen Flüssigkeitselektrolyten gebildet wird, und bei der Verringerung der Viskosität bei niedrigen Temperaturen, bei denen [EMIM][OTf] deutlich viskoser wird und die Ionenleitfähigkeit sinkt – ein Bereich der Forschung im Bereich der aktiven Materialtechnik.
Katalyse- und organische Syntheseanwendungen
[EMIM][OTf] hat produktive Anwendung als Reaktionsmedium und Cokatalysator in einer Reihe organischer Synthesen und katalytischer Transformationen gefunden, wo seine Eigenschaften als polares, nichtkoordinierendes Lösungsmittel mit vernachlässigbarem Dampfdruck praktische Vorteile gegenüber herkömmlichen organischen Lösungsmitteln bieten.
Säurekatalysierte Reaktionen
Das Triflat-Anion leitet sich von Trifluormethansulfonsäure ab – einer der stärksten bekannten Brønsted-Säuren – und [EMIM][OTf] kann unter bestimmten Bedingungen, insbesondere in Kombination mit Metalltriflat-Katalysatoren, einen milden Lewis-Säure-Charakter aufweisen. Es wurde als Co-Lösungsmittel und Aktivierungsmedium bei Friedel-Crafts-Alkylierungen, Diels-Alder-Cycloadditionen und Glykosylierungsreaktionen verwendet, wo seine Polarität geladene Übergangszustände und Ionenpaare stabilisiert, die Reaktionsgeschwindigkeit beschleunigt und in einigen Fällen die Selektivität im Vergleich zu herkömmlichen molekularen Lösungsmitteln verbessert.
Übergangsmetallkatalysierte Reaktionen
In [EMIM][OTf] gelöste oder immobilisierte Palladium-, Ruthenium- und Rhodiumkatalysatoren wurden für Kreuzkupplungsreaktionen, Hydrierungen und Carbonylierungschemie eingesetzt. Die ionische Flüssigkeitsphase immobilisiert den Katalysator und erleichtert die Produkttrennung durch Extraktion mit unpolaren Lösungsmitteln, während der Metallkatalysator in der ionischen Flüssigkeitsphase zur Wiederverwendung über mehrere Reaktionszyklen zurückgehalten wird – eine zweiphasige Katalysestrategie, die sich der Herausforderung der teuren Rückgewinnung und Wiederverwertung von Edelmetallkatalysatoren in der Feinchemiesynthese stellt.
Enzymatische und biokatalytische Prozesse
Eine wachsende Zahl von Forschungsarbeiten hat gezeigt, dass bestimmte Enzyme eine signifikante katalytische Aktivität behalten, wenn sie in [EMIM][OTf] oder [EMIM][OTf]-Wasser-Mischungen gelöst oder suspendiert werden. In diesem Zusammenhang wurden alle Lipasen, Proteasen und Oxidoreduktasen untersucht, wobei sich die relativ niedrige Viskosität und Wassermischbarkeit von [EMIM][OTf] als vorteilhaft für die Aufrechterhaltung der Enzymzugänglichkeit zu Substraten erwies. Die Fähigkeit, sowohl hydrophile als auch hydrophobe Substrate in einer einzigen ionischen Flüssigkeitsphase aufzulösen – unter Vermeidung der Phasentrennungsprobleme zweiphasiger wässrig-organischer Systeme – stellt einen bedeutenden praktischen Vorteil bei der biokatalytischen Synthese pharmazeutischer Zwischenprodukte und Feinchemikalien dar.
Anwendungen in der Materialwissenschaft und Nanotechnologie
[EMIM][OTf] wurde als funktionelles Medium in einer Reihe von Materialsynthese- und Nanotechnologieanwendungen eingesetzt, wo seine einzigartige Kombination von Eigenschaften Prozesse und Materialstrukturen ermöglicht, die mit herkömmlichen Lösungsmitteln nur schwer oder gar nicht zu erreichen sind.
- Galvanische Abscheidung von Metallen und Halbleitern: Das breite elektrochemische Fenster von [EMIM][OTf] ermöglicht die galvanische Abscheidung von Metallen wie Aluminium, Titan und Silizium, die aufgrund konkurrierender Wasserreduktionsreaktionen nicht aus wässrigen Elektrolyten abgeschieden werden können. Dies ermöglicht die Elektroabscheidung ionischer Flüssigkeiten als Weg zu funktionellen Metallbeschichtungen, Legierungen und Halbleiterdünnfilmen für Mikroelektronik- und Photovoltaikanwendungen.
- Nanopartikelsynthese: [EMIM][OTf] fungiert sowohl als Lösungsmittel als auch als stabilisierendes Medium für die Synthese von Metallnanopartikeln, wobei seine hohe Viskosität im Vergleich zu Wasser und starke Ionenpaarwechselwirkungen mit Nanopartikeloberflächen dazu beitragen, die Keimbildung und Wachstumskinetik zu kontrollieren und Nanopartikel mit engeren Größenverteilungen als in herkömmlichen Lösungsmitteln zu erzeugen.
- Polymerelektrolyte und Gelelektrolyte: [EMIM][OTf] wurde in Polymermatrizen – einschließlich Poly(vinylidenfluorid), Polyacrylnitril und Poly(ethylenoxid) – eingearbeitet, um flexible Gelpolymerelektrolyte für elektrochemische Festkörpergeräte, einschließlich flexibler Superkondensatoren, Festkörperbatterien und elektrochrome Geräte, herzustellen.
- Auflösung von Zellulose und Biomasse: Ionische Imidazolium-Flüssigkeiten, einschließlich [EMIM][OTf], zeigen die Fähigkeit, Zellulose und Lignozellulose-Biomasse aufzulösen und eröffnen Wege für die Verarbeitung dieser erneuerbaren Rohstoffe zu Mehrwertprodukten, einschließlich Biokraftstoffen, Spezialfasern und chemischen Bausteinen, unter milden Bedingungen ohne die aggressiven Säure- oder Basenbehandlungen, die bei herkömmlichen Zellstoffverfahren erforderlich sind.
Sicherheits-, Handhabungs- und Umweltaspekte
Während [EMIM][OTf] im Hinblick auf Brandgefahr und Inhalationsexposition erhebliche Sicherheitsvorteile gegenüber flüchtigen organischen Lösungsmitteln bietet, erfordert sein ökologisches und toxikologisches Profil eine sorgfältige Prüfung. Die Verbindung ist nach Standardklassifizierungen nicht akut toxisch, aber ionische Imidazoliumflüssigkeiten als Klasse haben bei erhöhten Konzentrationen eine ökotoxikologische Aktivität gegen Wasserorganismen gezeigt, wobei die Toxizität im Allgemeinen mit der Länge der Kation-Alkylkette zunimmt – die Ethylgruppe von [EMIM] ordnet sie dem niedrigeren Toxizitätsbereich der Imidazoliumreihe zu. Das fluorhaltige Triflat-Anion ist chemisch stabil und resistent gegen biologischen Abbau, was Bedenken hinsichtlich der langfristigen Umweltverträglichkeit aufwirft, wenn die Verbindung durch unsachgemäße Entsorgung in Gewässer gelangt.
Zu den empfohlenen Vorsichtsmaßnahmen bei der Handhabung gehören Standard-Labor-PSA – Nitrilhandschuhe, Schutzbrille und Laborkittel – mit besonderem Augenmerk auf die Minimierung des Hautkontakts aufgrund der Möglichkeit einer Hautabsorption. Die Entsorgung sollte den institutionellen Protokollen zur Entsorgung chemischer Abfälle folgen. Aufgrund seiner aquatischen Ökotoxizität und Persistenz sollte die Verbindung nicht in den Abfluss geschüttet werden. Es wird empfohlen, es in verschlossenen Behältern, fern von starken Oxidationsmitteln, starken Basen und Feuchtigkeit, aufzubewahren. Trotz dieser Überlegungen ist das allgemeine Umweltrisikoprofil von [EMIM][OTf] im Vergleich zu vielen herkömmlichen Lösungsmitteln günstig, insbesondere zu halogenierten Lösungsmitteln, deren Flüchtigkeit, Karzinogenität und Persistenz unter typischen Laborbedingungen schwerwiegendere Risiken für die Umwelt und die Gesundheit der Arbeitnehmer darstellen.
Auswahl von [EMIM][OTf] für Ihre Anwendung: Wichtige Entscheidungskriterien
[EMIM][OTf] ist keine universelle Lösung für jede Anwendung ionischer Flüssigkeiten, und eine fundierte Auswahl erfordert die Anpassung des spezifischen Eigenschaftsprofils an die Anwendungsanforderungen. Es ist die bevorzugte Wahl, wenn die folgenden Kriterien zutreffen:
- Eine niedrige Viskosität bei Raumtemperatur ist wichtig – [EMIM][OTf] gehört zu den weniger viskosen gängigen ionischen Flüssigkeiten und ist daher für vom Massentransport abhängige Prozesse den längerkettigen Imidazoliumtriflaten vorzuziehen
- Eine hohe Ionenleitfähigkeit ist erforderlich – seine Leitfähigkeit von ~8–9 mS/cm macht es zu einem der leitfähigeren RTILs und eignet sich für elektrochemische Anwendungen, bei denen die Minimierung des Innenwiderstands von entscheidender Bedeutung ist
- Wassermischbarkeit ist erforderlich – im Gegensatz zu hydrophoben ionischen Flüssigkeiten auf Basis von Bis(trifluormethylsulfonyl)imid (NTf₂) oder Hexafluorphosphatanionen ist [EMIM][OTf] wassermischbar und ermöglicht so wässrige Zweiphasensysteme und wasserbasierte Verarbeitungsschritte
- Ein moderates elektrochemisches Fenster ist ausreichend – wobei das ~4,1–4,3 V-Fenster von [EMIM][OTf] die Anforderungen erfüllt, ohne dass die breiteren Fenster erforderlich sind, die mit NTf₂-basierten ionischen Flüssigkeiten auf Kosten einer geringeren Leitfähigkeit erreichbar sind
- Im Handel erhältliches, gut charakterisiertes Material wird bevorzugt – [EMIM][OTf] ist bei Lieferanten von Spezialchemikalien in Forschungs- und Großmengen mit umfassenden Charakterisierungsdaten weit verbreitet, was den Beschaffungs- und Qualitätsüberprüfungsaufwand reduziert
Während sich die Wissenschaft über ionische Flüssigkeiten weiter von der akademischen Neugier zur industriellen Umsetzung weiterentwickelt, nimmt [EMIM][OTf] eine etablierte Position als Benchmark-Material ein – umfassend charakterisiert, zuverlässig synthetisiert und ausreichend vielseitig, um auf absehbare Zeit eine erste Wahl in den Bereichen Elektrochemie, Katalyse und fortschrittliche Materialverarbeitung zu bleiben.


 English
English Deutsch
Deutsch Español
Español 中文简体
中文简体